Duiding
Het effect van verschillende geneesmiddelen bij paniekstoornis
21 03 2023
Zorgberoepen
Apotheker, Huisarts, PsycholoogCiteer dit als : Catthoor K. - Het effect van verschillende geneesmiddelen bij paniekstoornis. Minerva Duiding 21/03/2023. Duiding van Chawla N, Anothaisintawee T, Charoenrungrueangchai K, et al. Drug treatment for panic disorder with or without agoraphobia: systematic review and network meta-analysis of randomised controlled trials. BMJ 2022;376:e066084. DOI: 10.1136/bmj-2021-066084
Achtergrond
De paniekstoornis is een frequent voorkomende psychiatrische aandoening met een geschatte life-time prevalentie tussen 1 en 5% en vaak gepaard gaand met andere psychiatrische en medische aandoeningen (1). Terwijl in alle eerdere edities van de Diagnostic and Statistical Manual of Mental Disorders (DSM) agorafobie (i.e. het vermijden van sociale situaties waarin paniek kan ontstaan) een diagnostisch onderdeel vormde van de paniekstoornis, zijn ze beide voor het eerst als aparte entiteit opgenomen in de DSM-5. Voor de behandeling van paniekstoornissen worden zowel farmacologische als psychotherapeutische interventies aanbevolen. In Minerva bespraken we enerzijds een studie die cognitieve gedragstherapie vergeleek met standaard psychotherapie (2,3) en anderzijds een studie die cognitieve gedragstherapie vergeleek met imipramine (4,5). We besloten dat op lange termijn cognitieve gedragstherapie de voorkeur geniet omwille van de afwezigheid van ongewenste effecten, maar dat de therapie niet voor elke patiënt geschikt is. Behalve tricyclische antidepressiva komen nog andere psychofarmaca in aanmerking voor de behandeling van de paniekstoornis.
Samenvatting
Methodologie
Systematische review met netwerk meta-analyse (6).
Geraadpleegde bronnen
- Medline via PubMed en Embase; tot juni 2021
- ClinicalTrials.gov voor nog lopende studies
- referentielijsten van geïncludeerde studies en vorige meta-analyses
- geen taalrestrictie.
Geselecteerde studies
- 87 gerandomiseerde gecontroleerde studies die het effect onderzochten van een interventie met psychofarmaca versus geen behandeling (placebo of wachtlijst) op vlak van remissie, studie-uitval, angstsymptomen, depressieve symptomen, levenskwaliteit en ongewenste effecten
- de onderzochte psychofarmaca bestonden uit (in afnemend aantal): tricyclische antidepressiva (TCA), selectieve serotonine-heropnameremmers (SSRI’s), benzodiazepines, serotonine-en-noradrenaline-heropnameremmers (SNRI’s, zoals venlafaxine), selectieve noradrenaline-heropnameremmers (zoals reboxetine), noradrenaline-en-dopamine-heropnameremmers (zoals buspirone (niet meer beschikbaar in België)), MAO-inhibitoren, bèta-blokkers, mirtazapine; de behandelduur bedroeg in 32 studies ≤8 weken en in 21 studies ≥12 weken
- exclusie van studies die verschillende dosissen van hetzelfde geneesmiddel vergeleken, alsook van studies met onvoldoende gegevens voor pooling of met gelijktijdige psychotherapie.
Bestudeerde populatie
- inclusie van 12 800 patiënten, 18 jaar of ouder (gemiddelde leeftijd van 35 jaar), 63,7% vrouwen, met een paniekstoornis (gediagnosticeerd volgens de DSM III, DSM III-R, DSM IV of ICD-10-criteria); 95% van de studies includeerde patiënten met agorafobie; de duur van de paniekstoornis bedroeg gemiddeld 6,9 jaar met een spreiding van 1,8 jaar tot 10,8 jaar.
Uitkomstmeting
- primaire uitkomstmaat: remissie (minstens een week geen paniekaanval meer op het einde van de studie) en studie-uitval (vroegtijdige stopzetting van de behandeling of terugtrekking uit de studie als gevolg van ongewenste effecten, overtreding van het studieprotocol of te weinig effect van de behandeling)
- secundaire uitkomstmaten: angst- en depressiesymptoomscores en elk mogelijk ongewenst effect
- directe meta-analyse wanneer minstens 3 RCT’s vergelijkbare interventies en uitkomstmaten evalueerden
- netwerk meta-analyse.
Resultaten
- voor de primaire uitkomstmaat ‘remissie’:
- in directe vergelijking met placebo was er statistisch significant meer remissie met tricyclische antidepressiva (TCA’s) (RR 1,37 met 95% BI van 1,27 tot 1,47; N=12; I²=0%), benzodiazepines (RR 1,49 met 95% BI van 1,36 tot 1,63; N=18; I²=13,18%), paroxetine (RR 1,42 met 95% BI van 1,12 tot 1,79; N=7; I²=55,77%), sertraline (RR 1,30 met 95% BI van 1,10 tot 1,54; N=3; I²=0%) en venlafaxine (RR 1,26 met 95% BI van 1,08 tot 1,48; N=4; I²=52,02%) maar niet met fluvoxamine (N=5; I²=71,69); er was geen verschil tussen TCA’s en benzodiazepines op vlak van remissie (N=6; I²=0%)
- in indirecte vergelijking met placebo was er statistisch significant meer remissie met tricyclische antidepressiva (TCA’s) (RR 1,39 met 95% BI van 1,26 tot 1,54; GRADE matig), benzodiazepines (RR 1,47 met 95% BI van 1,36 tot 1,60; GRADE matig), SSRI’s (RR 1,38 met 95% BI van 1,26 tot 1,50; GRADE matig), SNRI’s (RR 1,27 met 95% BI van 1,12 tot 1,45; GRADE matig) en MAO-inhibitoren (RR 1,30 met 95% BI van 1,00 tot 1,69; GRADE matig); er was meer remissie met benzodiazepines dan met bèta-blokkers (RR 1,98 met 95% BI van 1,03 tot 3,79; GRADE zeer laag) en SNRI’s (RR 1,16 met 95% BI van 1,00 tot 1,34; GRADE matig)
- voor de primaire uitkomstmaat ‘studie-uitval’:
- in directe vergelijking met placebo was er statistisch significant minder studie-uitval met tricyclische antidepressiva (TCA’s) (RR 0,42 met 95% BI van 0,31 tot 0,57; N=25; I²=71,69%) en benzodiazepines (RR 0,70 met 95% BI van 0,61 tot 0,79; N=20; I²=0%)
- in indirecte vergelijking met SSRI’s, SNRI’s, MAO-inhibitoren en placebo was er statistisch significant minder studie-uitval met benzodiazepines (RR met 95% BI resp. 0,51 (0,38-0,67), 0,57 (0,37-0,87), 0,47 (0,22-0,97) en 0,46 (0,37-0,58); GRADE matig); met TCA’s zag men een lagere studie-uitval versus SSRI’s (RR 0,78 met 95% BI van 0,61 tot 0,99) en placebo (RR 0,71 met 95% BI van 0,58 tot 0,88) (GRADE laag), maar een hogere studie-uitval versus benzodiazepines (RR 1,54 met 95% BI van 1,19 tot 1,99; GRADE laag)
- voor de secundaire uitkomstmaat ‘angstscore’:
- statistisch significante lagere angstscore na behandeling met TCA’s, benzodiazepines en paroxetine in directe vergelijking met placebo; alsook na behandeling met TCA’s, benzodiazepines, SSRI’s en SSRI’s gecombineerd met bèta-blokkers in indirecte vergelijking met placebo en na behandeling met TCA’s, benzodiazepines, SSRI’s en SNRI’s in indirecte vergelijking met SSRI’s gecombineerd met bèta-blokkers
- voor de secundaire uitkomstmaat ‘depressiescore’:
- statistisch significante lagere depressiescore na behandeling met benzodiazepines in directe vergelijking met placebo; alsook na behandeling met TCA’s, benzodiazepines, SSRI’s, en SSRI’s gecombineerd met bèta-blokkers in indirecte vergelijking met placebo en na behandeling met TCA’s, benzodiazepines, bèta-blokkers, MAO-inhibitoren, SSRI’s, noradrenaline-heropnameremmers en SSRI’s gecombineerd met benzodiazepines in indirecte vergelijking met SSRI’s gecombineerd met bètablokkers
- voor de secundaire uitkomstmaat ‘ongewenste effecten’:
- statistisch significant meer ongewenste effecten met benzodiazepines, TCA’s, en venlafaxine in directe vergelijking met placebo
- het gebruik van TCA’s was statistisch significant gecorreleerd met een hoger aantal ongewenste effecten in indirecte vergelijking met SSRI’s, SNRI’s, noradrenaline-heropnameremmers en placebo, alsook het gebruik van benzodiazepines versus SSRI’s, SNRI’s, noradrenaline-heropnameremmers en placebo; het gebruik van SSRI’s was statistisch significant gecorreleerd met een hoger aantal ongewenste effecten in vergelijking met placebo.
Besluit van de auteurs
Deze bevindingen suggereren dat SSRI’s een hoge mate van remissie geven met een laag risico van ongewenste effecten voor de behandeling van een paniekstoornis. Van alle SSRI’s zijn sertraline en escitalopram geassocieerd met een hoge remissie en een laag risico van ongewenste effecten. De bevindingen waren echter gebaseerd op studies met een matige tot zeer lage zekerheid van bewijs, meestal als gevolg van studiebias, inconsistentie en onnauwkeurigheid in het rapporteren van de resultaten.
Financiering van de studie
Geen.
Belangenconflicten van de auteurs
Geen.
Bespreking
Bespreking van de methodologie
Deze systematische review en netwerk meta-analyse werd gerapporteerd volgens de PRISMA-aanbevelingen. De onderzoekers geven gedetailleerd weer welke zoektermen en filters ze gebruikten voor hun zoektocht in PubMed en Embase. De zoektermen refereerden naar de bestudeerde populatie (zoals ‘paniekstoornis’ en ‘paniek’) en de interventie (zoals TCA, SSRI, SNRI). De selectie van artikels, de data-extractie en de evaluatie van de methodologische kwaliteit gebeurde door twee onafhankelijke onderzoekers. Op basis van de Cochrane risk of bias tool voor RCT’s bleek slechts één studie een laag risico van bias te hebben (gedefinieerd als een laag risico van bias voor alle domeinen). 29% had een hoog risico van bias (gedefinieerd als minstens één domein met een hoog risico van bias) en voor de meeste studies bestond er onduidelijkheid over hun risico van bias voor een of meerdere domeinen. Meestal was er een probleem met randomisatie en concealment of allocation, alsook met een selectieve rapportering van de resultaten. Wanneer er voor minstens drie RCT’s similariteit bestond in interventies en uitkomstmaten voerden de onderzoekers een directe meta-analyse uit. Daarnaast voerden de onderzoekers een netwerk meta-analyse uit (7,8). De consistentie van de resultaten werd statistisch onderzocht. Bij inconsistentie verwijderde men de studies die de inconsistentie veroorzaakten. Deze ingreep bleek alleen nodig voor de uitkomstmaat ‘ongewenste effecten’. Voor de resultaten van de netwerk meta-analyse werd de sterkte van het bewijs bepaald op basis van studiebias, rapporteringsbias, indirectheid, imprecisie, heterogeniteit en inconsistentie. Op basis van de indirecte vergelijkingen werd voor elke behandeling de SUCRA (Surface Under the Cumulative Ranking-curve) voor de verschillende uitkomstmaten berekend. Vervolgens zette men voor de primaire uitkomstmaten ‘remissie’ en ‘studie-uitval’ de SUCRA’s van de verschillende behandelingen tegenover elkaar uit. Er werden funnel plots gemaakt om publicatiebias en heterogeniteit op te sporen. Zo bleken de funnel plots voor de secundaire uitkomstmaten asymmetrisch te zijn. Dat zou echter meer te wijten zijn aan statistische heterogeniteit in plaats van aan publicatiebias.
Bespreking van de resultaten
Een van de sterktes van deze studie is dat veel psychofarmaca werden meegenomen in de meta-analyse en dat men zowel rekening hield met de positieve (remissie) als met de negatieve (studie-uitval, ongewenste effecten) effecten van de verschillende behandelingen. Op vlak van remissie vergeleek men meestal SSRI’s versus placebo (N=13 studies, n=2 295 patiënten), gevolgd door benzodiazepines versus placebo (N=11 studies, n=2 061 patiënten). Wat studie-uitval betreft, zag men de meeste vergelijkingen tussen benzodiazepines en placebo (N=15 studies, n=2 321 patiënten), gevolgd door SSRI’s versus placebo (N=14 studies; n=3 462 patiënten). Op basis van SUCRA rangschikte men benzodiazepines, tricyclische antidepressiva en SSRI’s bovenaan op vlak van remissie. Alhoewel de kans op studie-uitval het laagst was met benzodiazepines ging deze behandeling toch gepaard met de meeste ongewenste effecten. Ook met tricyclische antidepressie zag men meer ongewenste effecten dan met SSRI’s. Binnen de groep van SSRI’s bleken sertraline en escitalopram het meest effectief te zijn (op vlak van remissie) met de minste ongewenste effecten. Het is zeker nuttig om nog verder RCT’s te verrichten met directe vergelijkingen tussen meer recente SSRI’s, waarbij ook andere effecten zoals levenskwaliteit gemeten worden. Bij de bespreking van de resultaten moeten we rekening houden met het feit dat de effecten mogelijk overschat en de ongewenste effecten mogelijk onderschat zijn (zoals afhankelijkheid bij benzodiazepines). Omdat studies met psychotherapie werden uitgesloten, blijft het ook onduidelijk of er een meerwaarde is om psychofarmaca te combineren met sommige vormen van psychotherapeutische ondersteuning.
Wat zeggen de richtlijnen voor de klinische praktijk?
Ebp-net beveelt voor paniekstoornissen SSRI’s aan als eerstelijnstherapie, maar aan een startdosis die de helft bedraagt als voor de behandeling van een depressie. Benzodiazepines worden niet aanbevolen maar kunnen in de eerste fase van de farmacologische behandeling (wanneer paradoxale verergering van de klachten mogelijk is) tijdelijk toegevoegd worden. Ze moeten wel na maximaal 6 weken afgebouwd worden (9).
Besluit van Minerva
Deze systematische review met directe meta-analyse en netwerk meta-analyse toont aan dat de farmacologische behandeling van een paniekstoornis met SSRI’s gepaard gaat met een hoge mate van remissie en een laag risico van ongewenste effecten in vergelijking met andere psychofarmaca. Van alle SSRI’s zijn sertraline en escitalopram geassocieerd met het beste profiel op vlak van remissie en ongewenste effecten. De systematische review en meta-analyses zijn van goede methodologische kwaliteit, maar de geïncludeerde RCT’s vertonen wel een matig tot hoog risico van bias.
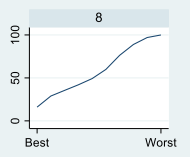
SUCRA (Surface under the Cumulatie Ranking-curve)
Men berekent de probabiliteit om als beste tot slechtste behandeling uit de analyse te komen. De oppervlakte onder de curve bepaalt de ranking van 0 (lage ranking) tot 100% (hoge ranking).
- de Jonge P, Roest AM, Lim CC, et al. Cross-national epidemiology of panic disorder and panic attacks in the world mental health surveys. Depress Anxiety 2016;33:1155-77. DOI: 10.1002/da.22572
- Luyten, P. Cognitieve gedragstherapie bij paniekstoornis: 2 jaar later. Minerva 2007;6(4):61-3.
- Addis ME, Hatgis C, Cardemil E, et al. Effectiveness of cognitive-behavioral treatment for panic disorder versus treatment as usual in a managed care setting: 2-year follow-up. J Consult Clin Psychol 2006;74:377-85. DOI: 10.1037/0022-006X.74.2.377
- De Meyere, M. Cognitieve gedragstherapie of imipramine bij paniekstoornis? Minerva 2001;30(10):464-7.
- Barlow DH, Gorman JM, Shear MK, Woods SW. Cognitive–behavioral therapy, imipramine, or their combination for panic disorder. A randomized controlled trial. JAMA 2000;283:2529-36. DOI: 10.1001/jama.283.19.2529
- Chawla N, Anothaisintawee T, Charoenrungrueangchai K, et al. Drug treatment for panic disorder with or without agoraphobia: systematic review and network meta-analysis of randomised controlled trials. BMJ 2022;376:e066084. DOI: 10.1136/bmj-2021-066084
- Chevalier P. Netwerk meta-analyses: directe en indirecte vergelijkingen. Minerva 2009;8(9):136.
- Chevalier P. Indirecte vergelijkingen (vervolg). Minerva 2011;10(6):77.
- Angststoornis. Ebp-net. Duodecim Medical Publications. Bijgewerkt door producent: 29/09/2011. Gescreend door Ebpracticenet: 2017.
Auteurs
Catthoor K.
psychiater psychosezorg ZNA PZ Stuivenberg, voorzitter Vlaamse Vereniging voor Psychiatrie
COI : Geen belangenconflicten met het onderwerp.
Trefwoorden
agorafobie, angst, antidepressivum, benzodiazepine, buspiron, depressie, dropout, inhibitor van het monoamineoxidase B, ongewenst effect, paniekstoornis, paroxetine, placebo, remissie, selectieve serotonine-heropnameremmer, serotonine- en noradrenaline-heropnameremmer, sertraline, SNRI, SSRI, TCA, tricyclisch antidepressivum, venlafaxineWoordenlijst
surface-under-the-cumulative-ranking-curveCodering
Commentaar
Commentaar