Organisatie voor Evidence-Based Practice
Non-inferioriteitsstudies: het nut, de beperkingen en de valkuilen
Minerva 2009 Volume 8 Nummer 6 Pagina 88 - 88
Zorgberoepen
Citeer dit als : Chevalier P. - Non-inferioriteitsstudies: het nut, de beperkingen en de valkuilen. Minerva Artikel 2009;8(6):88-88.
Nascholing: EBM begrippen
| In deze rubriek brengt de redactie korte teksten over gangbare begrippen in Evidence-Based Medicine (EBM). |
Non-inferioriteitsstudies, soms onterecht equivalentiestudies genoemd, zijn niet hetzelfde als superioriteitsstudies. Een behandeling X is niet inferieur aan een behandeling Y als het verschil tussen deze twee behandelingen binnen een vastgelegde klinische marge valt. Deze marge voor non-inferioreit (ΔC) is het resultaat van een afspraak onder experten en is gebaseerd op literatuuronderzoek, bij voorkeur op – indien beschikbaar - een meta-analyse. Ze moet kleiner zijn dan het afkappunt voor klinisch relevante superioriteit; over het algemeen wordt een waarde gekozen die de helft en soms tweederde bedraagt van het afkappunt voor superioriteit (1).
Illustratie
Nemen we verschillende non-inferioriteitsstudies, met een resultaat en betrouwbaarheidsinterval voor eenzelfde primair eindpunt op het vlak van werkzaamheid. Het resultaat (= het verschil tussen twee behandelingen) wordt weergegeven door een blokje en het 95% betrouwbaarheidsinterval van dit verschil door een horizontale lijn aan beide kanten van het blokje. Vergelijken we vervolgens de grenzen van deze betrouwbaarheidsintervallen met de vooraf afgesproken marge voor non-inferioriteit (ΔC). Om te kunnen spreken over non-inferioriteit moet de ondergrens van het betrouwbaarheidsinterval hoger zijn dan de vastgelegde non-inferioriteitsmarge (-ΔC).
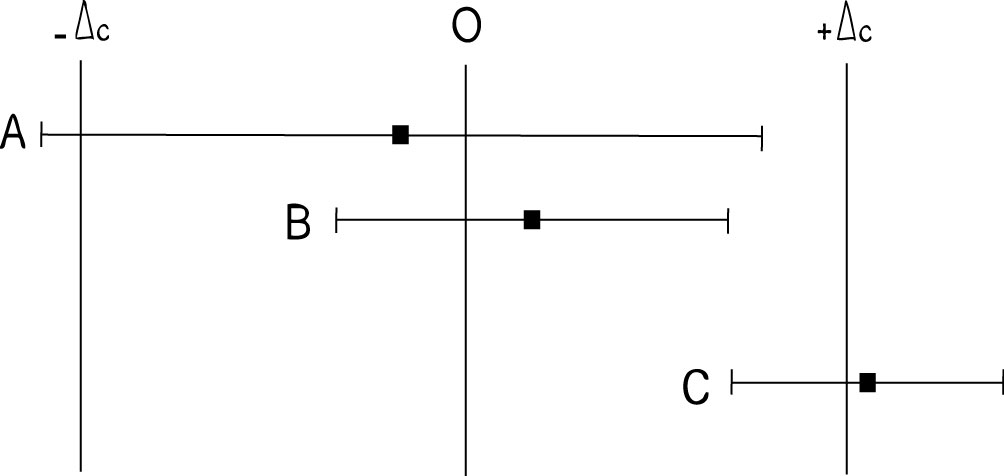
- in het voorbeeld A is er geen non-inferioriteit aangetoond tussen beide behandelingen
- in het voorbeeld B is er wel non-inferioriteit aangetoond
- in het voorbeeld C is het verschil tussen de twee behandelingen groter dan de vastgelegde non-inferioriteitsmarge (ΔC) en groter dan de equivalentiedrempel (O); non-inferioriteit is hier dus aangetoond en er kan zelfs sprake zijn van superioriteit (maar dit vereist andere toetsen).
Strikte methodologie
In vergelijking met de opzet van superioriteitsstudies moet de methodologie van non-inferioriteitsstudies aan enkele bijkomende voorwaarden voldoen. Deze zijn volgens McAlister en Sackett (2): een per protocol analyse (resultaten van de patiënten die werkelijk de behandeling volgden) bovenop een intention to treat analyse (resultaten van alle geïncludeerde patiënten), een bewezen effect van de behandeling in de controlegroep, dezelfde populatie en eindpunten als in vroegere studies waarbij een effect werd aangetoond, een strikte toepassing van het protocol, een aangepaste nulhypothese en een in het initiële protocol vastgelegde non-inferioriteitsmarge. Het bepalen van deze marge is onderwerp van discussie en sommige experten stellen voor om hierbij ook rekening te houden met de aard van de pathologie en met de te evalueren behandeling (3). We kunnen niet genoeg benadrukken dat de behandeling waarmee vergeleken wordt, bewezen effectief moet zijn. De steekproef van een non-inferioriteitsstudie moet groter zijn dan de steekproef van een superioriteitsstudie. Sommige experten spreken van 10% meer (4), anderen stellen een verhouding voor van één (superioriteit) op vier (non-inferioriteit), berekend op basis van een non-inferioriteitsmarge gelijk aan de helft van de superioriteitsdrempel (dit wordt zelden toegepast).
Van non-inferioriteitsprotocol naar superioriteitsprotocol
In 2008 publiceerde Minerva de bespreking van een studie met zowel een inferioriteits- als een superioriteitsprotocol (5). Roteren van een non-inferioriteitsprotocol naar een superioriteitsprotocol is mogelijk, wanneer aan verschillende voorwaarden wordt voldaan: het initiële non-inferioriteitsprotocol moet correct zijn, er moet een p-waarde berekend zijn om superioriteit aan te tonen en het resultaat moet statistisch significant zijn met een intention to treat analyse (6).
Betrouwbaarheid van non-inferioriteitsstudies
Kaul et al. onderzochten de validiteit van acht non-inferioriteitsstudies (negen publicaties) in het cardiovasculaire gebied (7). Zeven van de negen publicaties toonden zogezegd een non-inferioriteit aan. Kaul et al. analyseerden grondig alle gekozen non-inferioriteitsmarges en konden op die manier slechts voor vier van de acht studies een werkelijke non-inferioriteit aantonen. Nog veel andere auteurs benadrukken de talrijke methodologische beperkingen van non-inferioriteitsstudies (8).
Besluit
Het is niet mogelijk om bondig en eenduidig aanwijzingen te geven voor een goede interpretatie van de resultaten van non-inferioriteitsstudies; vooral de globale methodologische validiteit, de klinische relevantie van de gekozen marge en van de resultaten zijn elementen van evaluatie. Minerva zal elke non-inferioriteitsstudie voorzien van enkele gepaste commentaren.
- Grouin JM, Coste M. Essais de non-infériorité et d’équivalence: méthodologie et analyse. In Essais cliniques: théorie, pratique et critique. Médecine-Sciences Editions Flammarion 2006.
- McAlister FA, Sackett DL. Active-control equivalence trials and antihypertensive agents. Am J Med 2001;111:553-8.
- Regulatory watch: Non-inferiority-trial discussions impact new drug applications. Nat Rev Drug Discov 2009;8:10.
- Djulbegovic B, Clarke M. Scientific and ethical issues in equivalence trials. JAMA 2001;285:1206-8.
- Chevalier P. Na majeure electieve orthopedische ingreep: eerder rivaroxaban dan een heparine met laag moleculair gewicht? Minerva 2008;7(10):148-9.
- Committee for proprietary medicinal products (CPMP). Points to consider on switching between superiority and non-inferiority. EMEA CPMP/EWP/482/99.
- Kaul S, Diamond GA. Good enough: a primer on the analysis and interpretation of noninferiority trials. Ann Intern Med 2006;145:62-9.
- Le Henanff A, Giraudeau B, Baron G, Ravaud P. Quality of reporting of noninferiority and equivalence randomized trials. JAMA 2006;295:1147-51.
Commentaar
Commentaar





